Analiza Memoranduma o regulatornoj naučnoj politici FDA: proizvodi za verifikaciju starosti dobijaju prioritetnu reviziju, arome bez duhana moraju dokazati povećanje koristi
Ostavi poruku
Analiza Memoranduma o regulatornoj naučnoj politici FDA: proizvodi za verifikaciju starosti dobijaju prioritetnu reviziju, arome bez duhana moraju dokazati "postepenu korist"

Dana 21. novembra, FDA je izdala 13 naučnih memoranduma o politici o PMTA pregledu. 2Prvo je komunicirao s nekoliko stručnjaka za usklađenost i otkrio da će proizvodi e-cigareta s "tehnologijom provjere starosti" biti prvo pregledani; u isto vrijeme, FDA je otkrila da e-cigarete bez okusa duhana moraju dokazati "postepene prednosti" za odrasle pušače, a aplikacije koje ne pruže randomizirana kontrolirana ispitivanja ili podatke o dugoročnim istraživanjima mogu se smatrati "fatalnim nedostacima".
Američka uprava za hranu i lijekove (FDA) je 21. novembra izdala 13 memoranduma o naučnoj politici za reviziju aplikacija za e-cigarete prije stavljanja na tržište, u rasponu od 2020. do 2023. godine. FDA je rekla da ovi memorandumi opisuju proces i prioritetne metode koje se koriste za arhivirajte i pregledajte aromatizirane e-cigarete i druge PMTA (detalji: Američka FDA izdaje 13 memoranduma o regulatornoj naučnoj politici: Fokus na metode pregleda aromatiziranih e-cigareta).

FDA izdaje memorandum o regulatornoj naučnoj politici u vezi sa PMTA|Izvor: FDA
Što se tiče sadržaja ovog memoranduma objavljenog, 2First je konsultovao relevantne materijale i komunicirao sa mnogim stručnjacima za usklađenost i utvrdio da je važnost „tehnologije provjere starosti“ jasno navedena, odnosno da će uređaji s provjerom starosti dobiti prioritetnu reviziju. U isto vrijeme, neki memorandumi su također otkrili detalje o dodatnim zahtjevima FDA za istraživanje okusa u kasnijim pregledima.
Proizvodi s provjerom starosti mogu dobiti prioritetnu reviziju
Memorandum pod nazivom „Prioritet za podnošenje zahtjeva za PMTA primljene između 10. septembra 2020. do 3. novembra 2021.“ opisuje politiku FDA i pozadinu za davanje prioriteta primljenim prijavama za duhanske proizvode prije stavljanja na tržište (PMTA).

Podnošenje prioriteta za PMTA primljene u periodu od 10. septembra 2020. do 3. novembra 2021. Memorandum|Izvor: FDA
U memorandumu, FDA je objasnila ključne principe svojih prioriteta revizije, koji uglavnom uključuju sljedeća dva aspekta:
Na osnovu datuma podnošenja: PMTA se obično pregledaju po redoslijedu datuma podnošenja. Na primjer, proizvodi podneseni 10. septembra imat će prioritet u odnosu na prijave podnesene 15. septembra.
Posebni prioriteti: Neke aplikacije sa posebnim tehnologijama ili od značaja za javno zdravlje mogu imati prioritet. Na primjer, u memorandumu se izričito spominje da je kompanija podnijela PMTA sa "tehnologijom koja određuje starost", koja je bila prioritetna zbog potencijalnog uticaja na javno zdravlje. FDA je navela da je "aplikacija bila prioritetna za Podnošenje jer sadrži navodnu tehnologiju koja određuje starost."

"Aplikacija je dobila prioritet jer sadrži navodnu tehnologiju provjere starosti|Izvor: FDA
"Memorandum pokazuje činjenicu da se proizvodi sa "provjerom starosti" mogu brže pregledati i prošli drugi krug pregleda, direktno ulazeći u treću fazu pregleda." rekao je Kurt, konsultant za usklađenost u 2Firsts.
Kurt je rekao: "Shvatio sam da će FDA dati prioritet pregledu proizvoda za verifikaciju starosti i direktno ubrzati red do treće faze pregleda, ali standardi pregleda nisu smanjeni."
On također vjeruje da se logika FDA-e za pregled e-cigareta može vidjeti iz ovoga: uređaji s funkcijama provjere starosti mogu efikasno spriječiti tinejdžere da ih koriste, tako da se smatraju prioritetom.
Rekao je da takvi proizvodi možda neće morati proći skupa randomizirana kontrolirana ispitivanja (RCT) ili dugoročne kohortne studije (Longitudinal Cohort Studies), jer su njihovi terminalni uređaji već igrali preventivnu ulogu u zlostavljanju adolescenata.
Proizvodi okusa moraju dokazati "postepene prednosti"
U drugom memorandumu pod naslovom "ENDS koji sadrži e-tečnost bez arome duhana: pristup PMTA1 koji nije u suštinskom naučnom pregledu (faza III)", FDA je raspravljala o strategiji upravljanja primjenom duhanskih proizvoda prije stavljanja na tržište (PMTA) za e. -cigarete (ENDS).
U memorandumu, FDA je objasnila svoje standarde pregleda. Agencija je citirala član 910 američkog Federalnog zakona o hrani, lijekovima i kozmetici (FD&C Act). Da li je proizvod pogodan za "zaštitu javnog zdravlja" (APPH) ključno je za pregled. Elektronske cigarete bez arome duhana moraju dokazati da imaju "inkrementalne prednosti" (inkrementalne koristi) za odrasle pušače u usporedbi s proizvodima s aromom duhana. korist).
"Inkrementalna korist" se može shvatiti kao FDA koja zahtijeva od podnosilaca e-cigareta bez duhana da dokažu da pružaju dodatne prednosti odraslim pušačima u usporedbi s proizvodima s aromom duhana ili drugim postojećim opcijama, a za procjenu su potrebni dokazi iz randomiziranih kontroliranih ispitivanja (RCT-ovi). ) ili dugoročne kohortne studije.
Ako aplikaciji nedostaje gore navedeno istraživanje, to će se smatrati "fatalnom greškom" i može rezultirati marketinškim nalogom za odbijenicu (MDO).

Opis "fatalne mane"|Izvor: FDA

Opis "fatalne mane"|Izvor: FDA
Kurt je rekao da je od jula 2021. FDA dodala zahtjeve za dugoročna klinička ispitivanja za okuse u proces revizije. Ovaj dodatni zahtjev doveo je do toga da veliki broj kompanija bude ocijenjen nekvalifikovanim, a hiljade naloga za odbijanje tržišta izdato je kompanijama. Nakon toga, ove kompanije su podnijele više tužbi protiv FDA, tvrdeći da ovaj dodatni zahtjev krši originalne standarde revizije PMTA.
Dakle, kako FDA definira "arome bez duhana"?
Memorandum pod naslovom „Dodatak pristupu PMTA1 za ENDS2 koji nije sa aromom duhana2 koji nije u suštinskom naučnom pregledu (faza III)“ pruža odgovor. FDA u ovom podmemorandumu jasno navodi koji proizvodi pripadaju aromama bez duhana i definira opseg aroma "duvan" i "menta".
Kurt je rekao da arome duhana i arome mentola na ove dvije liste neće biti razmatrane kao proizvodi okusa. Samo FLAVOR SKU će biti predmet dugoročnog pregleda kliničkog ispitivanja sa fatalnim nedostatkom. Ako nema relevantnih dokaza, FDA će im poslati MDO pismo.
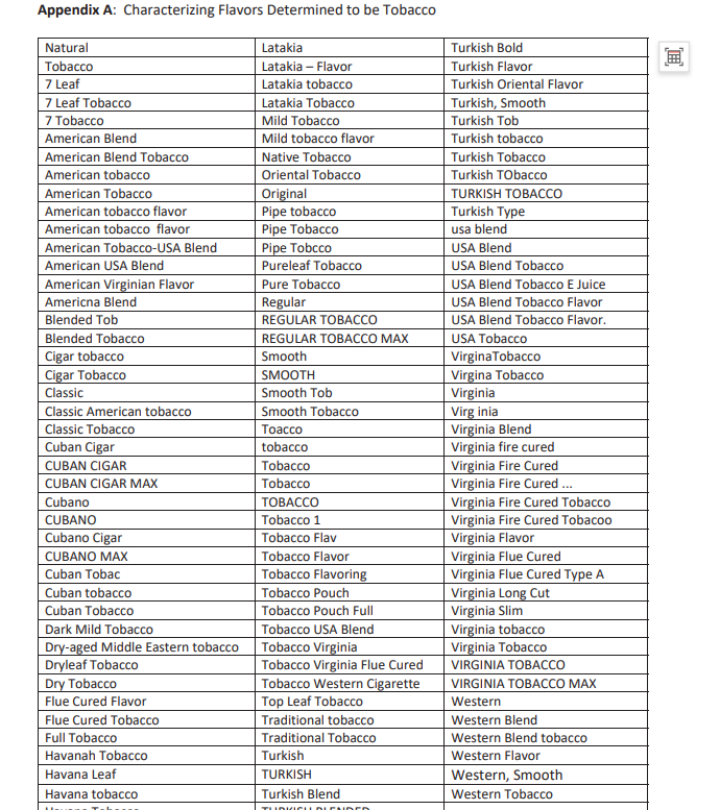
Lista dopisa o e-cigaretama s okusom duhana koji nisu prošli suštinsku naučnu recenziju|Izvor: FDA

Lista dopisa o e-cigaretama s okusom duhana koji nisu prošli suštinsku naučnu recenziju|Izvor: FDA

Priložena lista memoranduma o e-cigaretama s okusom duhana koji nisu prošli suštinsku naučnu recenziju|Izvor: FDA
Ovo je četvrta serija memoranduma izdanih 2024. godine, a FDA je izdala ukupno 26 memoranduma o regulatornoj naučnoj politici. Iako je FDA navela da objavljeni memorandumi ne bi trebali biti korišteni kao alati, smjernice ili priručnici za pripremu aplikacija ili podnošenje dokumenata FDA. Međutim, analiza i tumačenje ovih memoranduma i dalje pomaže da se ima dublje i preciznije razumijevanje FDA-ove filozofije i metoda za pregled e-cigareta.
Dvojica vrhovnika će nastaviti da obraćaju pažnju na najnovija dešavanja u američkoj regulatornoj politici e-cigareta.









